Содержание
- 1 Ответ
- 2 Номенклатура спиртов
- 3 Одноатомные спирты
- 4 Метанол как продукт природного газа
- 5 Получение предельных спиртов из алкенов
- 6 Косвенный способ гидратации этилена
- 7 Спиртовое брожение
- 8 Способы получения алкогольных напитков
- 9 Реакция нуклеофильного замещения
- 10 Нуклеофильное присоединение.
- 11 Реакция восстановления
Получают этиловый спирт тремя способами:
- · ферментативным (брожением пищевого сырья или биохимическим),
- · химическим (гидролиз растительного сырья)
- · синтетическим (гидратация этилена).
В первом случае происходит сбраживание сахара под действием ферментов, дрожжей:
Во втором случае вырабатывают технический спирт из растительного сырья с высоким содержанием клетчатки негидролизуемыми ферментами дрожжевой клетки (древесных опилок, соломы, торфа, мха и т. п.) и из сульфитных щелоков (отходов целлюлозно-бумажного производства), содержащих до 1,5% сахара, химическим способом воздействуя на сырье минеральными кислотами.
В третьем случае получают технический синтетический спирт путем присоединения к этилену воды в присутствии катализатора:
В качестве сырья для получения этилового спирта используются как пищевые, так и непищевые продукты в зависимости от назначения получаемого спирта. Пищевой спирт производится только из пищевого сырья. Сырьем для производства спирта являются зерновые – пшеница, рожь, ячмень, овес, кукуруза, просо, а также сахарная свекла, сахарная патока или меласса и картофель. Значительно реже используются плодово-ягодные, виноградные материалы, топинамбур и другое богатое углеводами сырье.
Технический спирт получают из древесины или нефтепродуктов, подвергаемых кислотному гидролизу. Технический спирт содержит повышенное количество вредных примесей, поэтому использование его для пищевых целей запрещено.
Классификация этилового спирта
Виды этилового спирта в зависимости от используемого сырья:
- · Пищевой спирт
- · Технический спирт
- · Картофельный
- · Древесный
- · Пшеничный
- · Гидролизный
- · Ржаной
- · Синтетический
- · Кукурузный
- · Просяной
- · Овсяный
- · Свекловичный
- · Сахарно-мелассовый
Сорта в зависимости от степени очистки:
Выход абсолютного спирта со 100 кг различных видов сырья (с учетом потерь) представлен в таблице 1
Таблица 1 Количество получаемого спирта из 100 кг сырья
Кол-во получаемого спирта, л/100 кг
Топинамбур (Земляная груша)
Производство спирта из сахарсодержащего сырья
В последние годы все большее внимание уделяется производству спирта из сахарсодержащего сырья и использованию его в качестве альтернативного горючего, так называемого, биоэтанола. Обычный топливный этанол, представляющий собой спирт, получают ферментацией сахара, а биоэтанол – ферментацией углеводов, добываемых из возобновляемых источников сырья: сахарной свеклы, пшеницы или ячменя. При сгорании этанола выделяется в несколько раз меньше углекислого газа, чем при сгорании бензина, а углекислый газ – одна из причин парникового эффекта и глобального потепления.
В настоящее время ежегодно в мире производится 330 млн гл спирта, при этом 60% его вырабатывается из сахарсодержащего сырья, 33% – из крахмалсодержащего и только 7% приходится на долю синтетического спирта. 13% производимого спирта используется для пищевых целей, 21 – для промышленных (химическая, косметическая и фармацевтическая промышленности), а остальные 66% – в качестве топлива для двигателей.
Мотивов производства спирта из свеклы в качестве альтернативного источника топлива можно назвать несколько: повышающиеся цены на нефть и газ, а также политические аспекты. Считается, что 1 л этанола эквивалентен примерно 0,67 л бензина.
Согласно расчетам специалистов, энергетическая эффективность производства спирта из сахарной свеклы, с учетом ее выращивания, составляет 173% (отношение произведенной энергии к затраченной).
Производство спирта этилового ректификованного пищевого состоит из следующих этапов:
¦ подготовительного — очистка сырья от примесей, приготовление солода;
¦ основного — разваривание крахмалистого сырья, осахаривание крахмала, сбраживание осахаренной массы, перегонка бражки и получение сырого спирта;
¦ завершающего — ректификация (повторная перегонка с целью очистки этилового спирта от примесей).
Спирт из любого органического сырья
Американская компания Coskata разработала новый процесс производства этилового спирта, позволяющий применять практически любое органическое сырье, включая твердые бытовые отходы, старые покрышки, отходы деревообработки и сельского хозяйства и т.п. [Voegele, E. November 2009. “Waste to ethanol projects move forward”, Ethanol Producer Magazine]
По заявлениям Coskata, стоимость литра спирта, полученного с помощью новой технологии, составит около 26 центов (1 доллар за галлон).
Основным применением технологии должно стать производство спирта для использования в качестве моторного топлива. В настоящее время в США для выпуска спиртового топлива, часто называемого биоэтанолом, используется растительное сырье, прежде всего кукуруза. Однако такой спирт достаточно дорог, кроме того использование посевных площадей для "биотопливных" культур ведет к росту цен на продовольствие. Поэтому все больший интерес проявляется в производству топливного этанола из непищевого сырья.
Основным достижением Coskata стало объединение в одной технологической цепочке традиционной химической и биотехнологии. На первой стадии процесса сырье подвергается газификации – в присутствии катализатора органические молекулы превращаются в синтез-газ – смесь моноксида углерода (СО) и водорода. Синтез-газ давно и достаточно широко используется в химической промышленности, прежде всего для производства другого спирта – метанола. Кроме того, из синтез-газа можно получать углеводороды и другие ценные химические соединения.
В Coskata синтез-газ используется для получения этилового спирта. При этом в компании отказались от традиционных катализаторов и заменили их специально подобранными бактериями – именно в них кроется основное "ноу-хау" процесса, а разработчики называют бактерий не иначе как "проприетарными".
Бактерии, обитающие в биореакторе, питаются синтез-газом и выделяют этанол высокой чистоты, тогда как на традиционных катализаторах обычно получается смесь спиртов, требующая дополнительного разделения и очистки. Кроме того, бактерии не столь чувствительны к каталитическим ядам (например, соединениям серы), что позволяет удешевить процесс, избавившись от стадий очистки сырья.
Разработки Coskata уже привлекли внимание автомобильной отрасли. Поддержку в промышленной реализации процесса начинающей компании окажет концерн General Motors.
Для получения синтетического этанола сырьём служит этилен, который подвергают сернокислотной гидратации или гидратации на твёрдых фосфорно-кислотных катализаторах (прямая гидратация):
С2Н4 + Н2SO4 > C2H5OSO3H + H2O > C2H5OH + Н2SO4
Процесс производства этилового спирта сернокислотной гидратацией этилена показан на рис
Этилсульфаты и серная кислота из абсорбера 1 поступают в гидролизер 6, в который подается вода. В гидролизере при давлении 1 МПа и температуре 70–90 °С происходит гидролиз этилсульфатов:
C2H5OSO3H + H2O C2H5OH + Н2SO4

Рис. 3 Схема производства этилового спирта сернокислотной гидратацией этилена: 1– тарельчатый абсорбер; 2, 3 — скрубберы; 4 — холодильник; 5 — колонна; 6 — гидролизер
Пары спирта и воды далее проходят холодильник 4, где они конденсируются; конденсат поступает в ректификационную колонну 5 для разгонки и очистки от примесей. Разбавленная кислота (50%) выводится из гидролизера, направляется на концентрирование и снова возвращается в процесс. При ректификации концентрация этилового спирта достигает 95–96%. По этому способу из 1 т этилена получают 1,2 т этанола и около 100 кг этилового эфира.
Основные физико-химические свойства метилового и этилового спиртов как топлив приведены в таблице 2.
Таблица 2 Физико-химические свойства основных спиртов как топлив
Ответ

Из этанола получить этаналь очень просто: просто окислив этанол.
С2Н5ОН + 2CuO –> СН3СНО + Cu2O + H2O
Я взял оксид меди, так как это слабый окислитель, и его хватит чтобы окислить этанол до этаналя.
А вот чтобы получить уксусную кислоту из этанола, можно взять более жёсткий окислитель, например KMnO4.
C2H5OH –>(над стрелочкой KMnO4) CH3COOH.
Если вы пишите окислитель над стрелочкой, то все продукты реакции можете не писать, а просто основное полученное вещество.
Полную реакцию вы можете поискать в интернете, если вам нужны все продукты реакции.
Спирты распространены в природе. Большинство людей знакомы с этиловым спиртом (этанолом) – активным ингредиентом алкогольных напитков, но он является лишь одним из семейства органических соединений, известных как спирты. Получение их, прежде всего этилового (винного в результате ферментативного брожения виноградного сока стало одним из первых химических техпроцессов, освоенных человечеством.
Номенклатура спиртов
Спирты представляет собой органические соединения гидроксильной (ОН) функциональной группы с алифатическим атомом углерода. Поскольку ОН является принадлежностью молекул всех спиртов, их часто представляют как производными воды с общей формулой ROH, где R обозначает алкильную группу.
Получение спиртов метанола (СН3ОН) и этанола (СН3СН2ОН), являющихся первыми двумя членами их гомологического ряда, является важной задачей химической промышленности многих стран. При содержании от одного до четырех атомов углерода их часто называют общими именами, в которых за названием алкильной группы следует слово спирт:
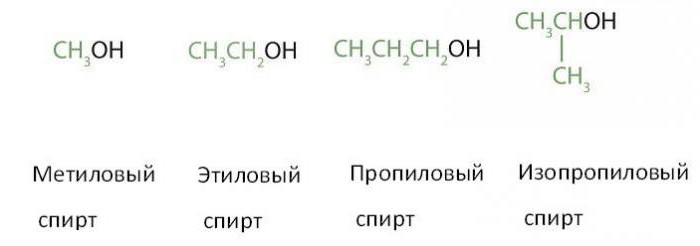
Можно видеть, что все четыре (две последние являются изомерами одного вещества) представленные выше молекулы спиртов содержат одну гидроксильную группу. По этому признаку все они относятся к классу одноатомных спиртов (бывают и двух-, трех, четырех- и многоатомные). Кроме того, все они являются производными предельных углеводородов из ряда алканов: метана, этана, пропана (названия спиртов получают добавлением к названию алкена окончания «-ол»). Поэтому их еще называют предельными одноатомными спиртами.
Одноатомные спирты
Получение, свойства (как физические, так и химические) этих соединений зависят от количества атомов углерода, присоединенных к его же атому, непосредственно связанному с группой ОН. Поэтому одноатомные спирты могут быть сгруппированы в три класса на этой основе.
-
Первичные спирты имеют молекулу, в которой один атом углерода, связанный с ОН-группой, присоединен к еще одному атому C. Их общая формула RCH2ОН. Например, этанол – первичный спирт.
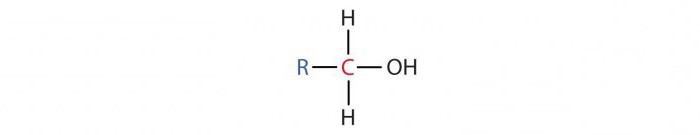
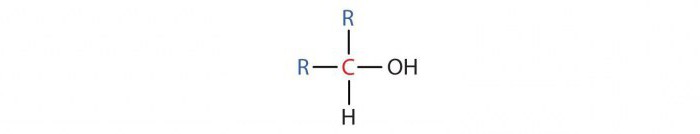

Получение одноатомных спиртов в промышленности возможно целым рядом способов, которые будут рассмотрены ниже.
Метанол как продукт природного газа
Метанол получают смешиванием газа водорода и монооксида углерода при высоких температурах и давлениях (200 ат, 350 °C) в присутствии катализатора, состоящего из оксида цинка (ZnO) и оксида хрома (Cr2 O3) в качестве катализатора: 2H2 + CO → CH3OH.

При этом сырьем для получения реагентов являются природный газ и водяной пар, смешивая которые, получают синтез – газ, представляющий собой смесь CO и H2.
Метанол является важным растворителем и используется в качестве автомобильного топлива, либо в виде чистой жидкости – в некоторых гоночных автомобилях, либо в качестве высокооктановой добавки в бензин. Получение и применение спиртов в мире, и в частности метанола, измеряется миллионами тонн. По итогам 2013 г. в мире было потреблено 66 млн т метанола, из них 65 % в Азии, 17 % – в Европе и 11 % – в США.
Получение предельных спиртов из алкенов
Многие простые весовые спирты, имеющие промышленное значение, производятся гидратацией (добавлением воды) алкенов (этилена, пропилена, бутена). Этанол, изопропанол, бутанол (вторичный и третичный) получают по этой реакции.
Известны прямой и косвенный способы получения спиртов гидратацией. Прямой позволяет избежать образования стабильных промежуточных продуктов, как правило, с помощью кислых катализаторов.
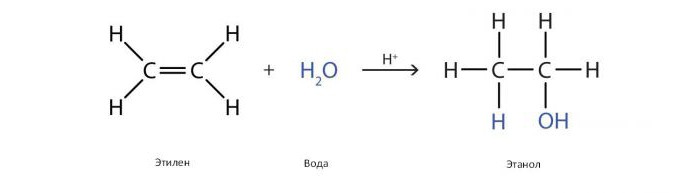
Катализатором обычно является фосфорная кислота, адсорбированная на пористом носителе, таком как силикагель или кизельгур. Этот катализатор был впервые использован для крупномасштабного производства этанола в США компанией "Шелл" в 1947 году. Реакцию проводят в присутствии пара высокого давления при 300 °C, причем между этиленом и паром поддерживается соотношение 1,0: 0,6.
Аналогичная реакция производства изопропилового спирта с катализаторов в виде серной кислоты выглядит следующим образом
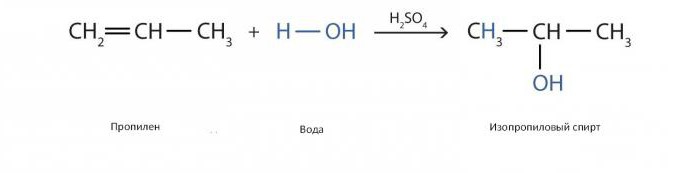
Косвенный способ гидратации этилена
В косвенным способе, на практике впервые примененном в промышленном масштабе в 1930 году, но сегодня считающимся почти полностью устаревшим, реакция получения спиртов заключается в превращении алкена в сульфат эфиры, который затем гидролизуют. Традиционно алкен обрабатывают серной кислотой с получением алкильные сульфатных эфиров. В случае производства этанола, этот шаг может быть записан так: Н2SO4 + С2 Н4 → C2H5 -O-SO3H
Впоследствии этот сульфат эфира гидролизуют до регенерации серной кислоты и освобождения этанола: С2Н5-O-SO3H + H2O → H2SO4 + С2Н5ОН.
Способы получения спиртов чрезвычайно разнообразны, но нижеописанный процесс, пожалуй, известен, хотя бы понаслышке каждому читателю.
Спиртовое брожение
Это биологический процесс, в котором молекулы, такие как глюкоза, фруктоза и сахароза, преобразуются в клеточную энергию с параллельным производством этанола и углекислого газа в качестве продуктов метаболизма. Брожение катализируется ферментами, содержащимися в дрожжах и протекает по сложному многоступенчатому механизму, которое включает в общем случае преобразование (на первом этапе) крахмала, содержащегося в растительных зернах, в глюкозу с последующим получением из нее этанола. Поскольку дрожжи выполняют это преобразование в отсутствие кислорода, спиртовое брожение считается анаэробным процессом.
Реакции получения спиртов брожением можно представить следующим образом:
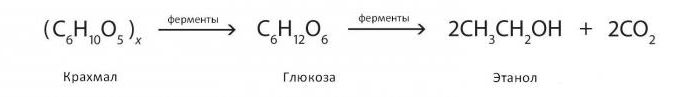
Способы получения алкогольных напитков
Весь этанол, содержащийся в алкогольных напитках производится посредством ферментации, вызванной дрожжами.
Вино производится путем ферментации из натуральных сахаров, присутствующих в винограде; сидр получают аналогичной ферментацией природного сахара в яблоках и грушах, соответственно; и другие фруктовые вина производятся ферментацией сахаров в любых других видах фруктов. Бренди и коньячные спирты (например, сливовица) производятся при перегонке напитков, получаемых брожением фруктовых сахаров.
Медовые напитки производятся путем ферментации из натуральных сахаров, присутствующих в меде.
Пиво, виски, и водка производятся путем ферментации зерен крахмала, которые преобразуются в сахар под действием фермента амилазы, присутствующей в зерновых ядрах, подвергшихся солодовому проращиванию. Другие источники крахмала (например, картофель и не солодовое зерно) могут быть добавлены к смеси, так как амилаза будет действовать также и на их крахмал.
Рисовые вина (в том числе саке) получают путем брожения зерновых крахмалов, превращаемых в сахар грибками Aspergillus огугае.
Ром и некоторые другие напитки получают ферментацией и дистилляцией сахарного тростника. Ром, как правило, производится из продукта сахарного тростника – патоки.
Во всех случаях брожение должно происходить в сосуде, который позволяет двуокиси углерода выходить, но предотвращает приход наружного воздуха. Это нужно потому, что воздействие кислорода предотвращает образование этанола, а накопление диоксида углерода создает риск разрыва сосуда .

Реакция нуклеофильного замещения
Получение спиртов в лабораториях производится способами, которые используют в качестве исходных продуктов для реакций химические вещества самых разнообразных классов, от углеводородов до карбонильных соединений. Существует несколько способов, которые сводятся к нескольким основным реакциям.
Первичные галогеналканы реагируют с водными растворами щелочей NaOH или КОН, образуя, образуя, главным образом, первичные спирты в реакции нуклеофильного алифатического замещения. Когда, например, метилбромид реагирует с раствором едкого натра, то гидроксильные группы, образующинся при диссоциации щелочи, замещают ионы брома с образованием метанола.
Несколько реакций, позволяющих выполнять получение спиртов в лабораториях, приведены ниже.
Нуклеофильное присоединение.
Реактивы Гриньяра (соединения магния с алкилгалогенидами – иодидами или бромидами), а также металлоорганические соединения меди и лития реагируют с карбонильными группами (C=O) альдегидов с образованием первичных и вторичных спиртов в зависимости от механизма присоединения.Аналогичные реакции с кетонами приводят к третичным спиртам.
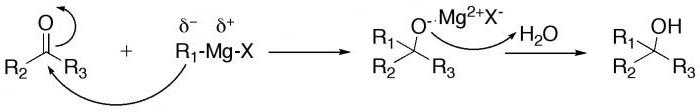
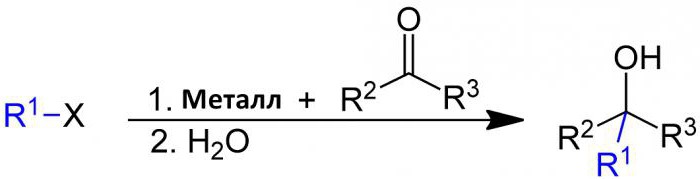
Реакция Барбье протекает между галогеналканом и карбонильной группой в качестве электрофильного субстрата в присутствии магния, алюминия, цинка, индия, олова или его солей. Продуктом реакции является первичный, вторичный или третичный спирт. Механизм ее протекания аналогичен реакции Гриньяра с той разницей, что реакция Барбье является синтезом в одном сосуде, тогда как реактив Гриньяра получают отдельно перед добавлением карбонильного соединения.
Реакция восстановления
Альдегиды или кетоны восстанавливаются до спиртов с боргидридом натрия (NaBH4) или (после кислотной обработки) с литийалюминий гидридом (LiAlH).
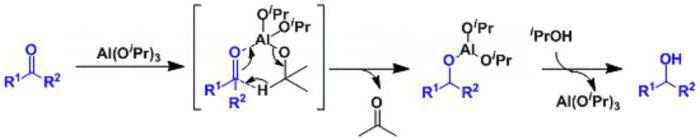
В реакции Меервейна-Пондорфа-Верли (MPV) получение спиртов путем восстановления их из кетонов и альдегидов происходит с использованием алюминиевого алкоксидного катализатора. Достоинства MPV заключаются в ее высокой хемоселективности и использовании дешевого, экологически чистого металлического катализатора. Реакция была обнаружена Меервейном и Шмидтом, и независимо Верли в 1925 г. Они обнаружили, что смесь алюминиевого этоксида и этанола может восстановить альдегиды до их спиртов. Понндорф применил реакцию к кетонам и обновил катализатор до изопропилата алюминия (Al(O-i-Pr)3, где i-Pr означает изопропиловую группу (CH(CH3)2). в целях получения изопропанола.
Общее уравнение получения спирта путем MPV-восстановления кетонов до спиртов выглядит так:
Это, конечно, не все, что можно сказать относительно спиртов и их свойств, но общее представление о них, надеемся, вам составить удалось.



